埃克森(北京)科技有限公司
11 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
- 查看全部分类
- Leica/徕卡
- Terumo/泰尔茂
- NIGALE/南格尔
- NIPRO/尼普洛
- WEGO/威高
- JD/金碟
- Thermobrite/雅培
- BASO/贝索
- BGI/吉诺因
- Feather/羽毛
- Miltenyi/美天旎
- LAISHI/莱士
- Nalgene/耐洁
- Applitech/艾贝泰
- Abm/爱必梦
- BD/碧迪
- Corning/康宁
- EASE/伊姿
- Illumina/因美纳
- SECA/赛康
- Abmole/奥默
- SAKURA/樱花
- VIOX Scientific
- Cytiva/思拓凡
- Esunbio/奕杉
- Marabu/玛莱宝
- Cargille
- Bms/佰美斯
- Fluidigm/富鲁达
- OLYMPUS/奥林巴斯
- Biosafe
- GIBCO
- Envision
- Serumwerk
- Biorep
- 多重免疫组化技术服务
- BioGems
- eBioscience
- MultiSciences/联科
- 首宁生物
- Thermo Scientific
- 赛百科洁
- 美国Scientific Industries
- Sigma
- Biotopped
- BIOFOUNT
- TBD
- Aicon-Bio
- ThermoFisher
- 唯公
- 莎斯特SARSTEDT
- LONZA
- PALL
- Millipore/密理博
- Greiner/格瑞纳
- Kemesser/科默斯
- EXSSON
- Sexton
- HELIOS
推荐产品
公司新闻/正文
Spectra Optia全面助力血液疾病治疗
937 人阅读发布时间:2024-08-30 15:16

在现代医学不断发展的背景下,血液疾病的治疗正逐步进入一个崭新的时代,伴随着单倍体相合造血干细胞移植的普及、CAR-T细胞疗法的兴起、血液成分单采术的广泛应用,血液成分分离设备在这一领域扮演着不可或缺的角色。Spectra Optia作为新一代血液成分分离设备,凭借其细胞采集能力和多性能为众多血液疾病患者带来了新的希望。本文将从移植物成分对异基因造血干细胞移植(allo HSCT)预后的影响、淋巴细胞采集对CAR-T治疗的价值以及单采术对血液疾病治疗的助力,全面探讨血液成分分离设备在血液疾病治疗中的价值。
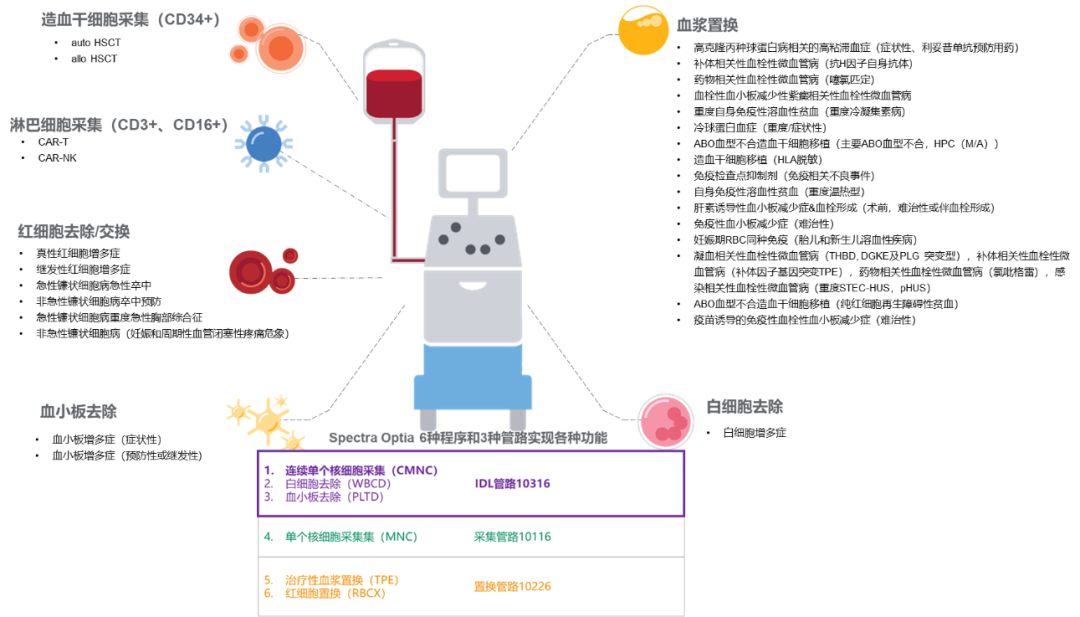
1. 移植物细胞成分与allo HSCT预后息息相关
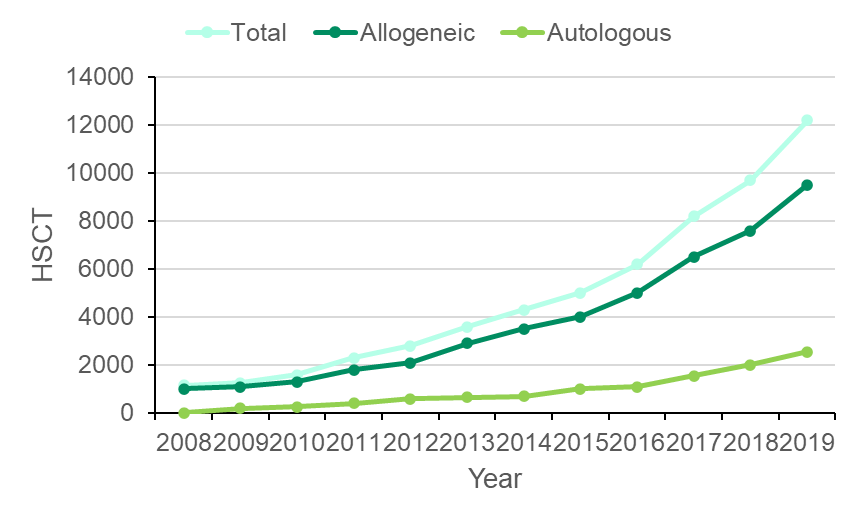
2008-2019年中国HSCT呈稳定增长态势,共报告了58,914例 HSCT,其中79%为异基因移植(allo HSCT)。异基因移植快速增长得益于中国医学界在单倍体相合造血干细胞移植(Haplo-HSCT)领域的创新突破,成功解决了供血者来源匮乏的全球性难题。自2013年以来,单倍体供体(HID)成为我国异基因供体中最主要的干细胞来源,2021年单倍体供体的使用率高达63%。
allo HSCT的快速增长也引发血液科医生关注移植物中各种细胞成分对allo HSCT的深远影响:CD34+细胞数量直接关系到移植后的造血恢复、复发风险及生存率,ABO血型不相容可导致多种并发症,粒细胞与GVHD、CMV激活等事件相关等。
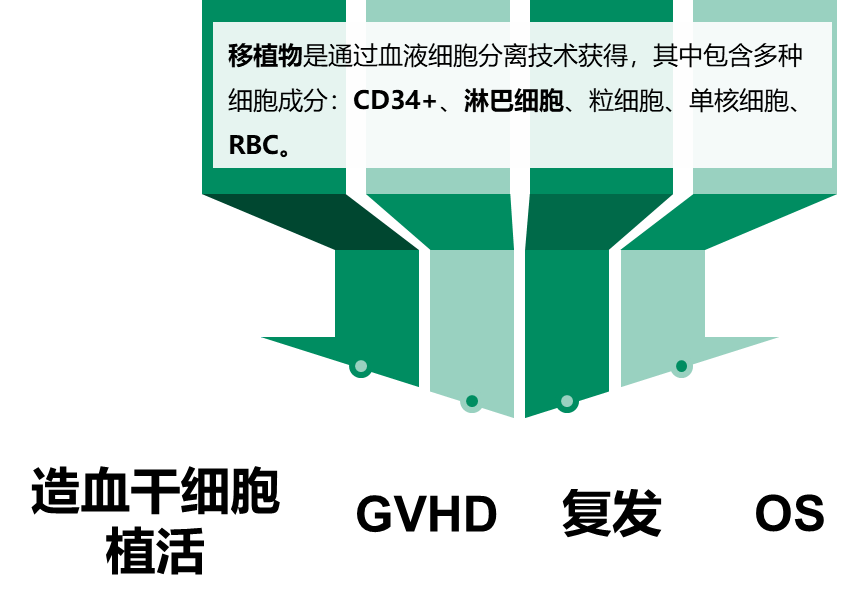
1.1 CD34+细胞数量与allo HSCT植活密切相关
CD34+细胞数量对移植后造血系统重建至关重要,国内外指南共识一致推荐2x106/kg作为输注CD34+细胞数的最低阈值,CD34+数量越多越利于造血干细胞的植活,但同时还需要考虑对a/c GVHD、疾病复发率及OS的影响,所以,allo HSCT输注CD34+数量最佳阈值一致处于探索之中。
一项回顾性研究纳入1,054名2002年至 2011年期间接受第一次异体移植和降低强度/非清髓预处理方案的45至75岁的 AML 或 MDS患者,研究人群仅限于患有 AML 或 MDS 的患者,这是老年患者同种异体移植的最常见适应症。多因素分析结果显示,HLA匹配的同胞供者移植中 CD34+数量<4×106/kg 与较低的中性粒细胞(OR 0.76,p=0.03)及血小板(OR 0.76,p=0.03)恢复相关;无关供者移植中 CD34+ 数量 <6×106/kg 的与移植受体较低的血小板(OR 0.87,p=0.03)恢复相关。
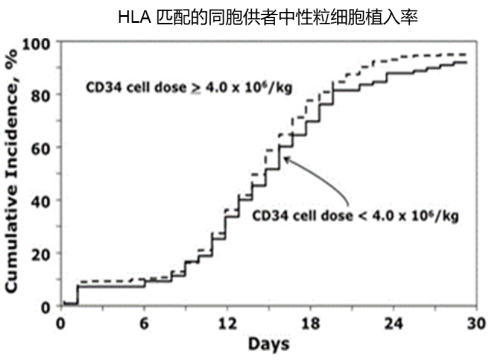
另一项回顾性研究纳入2002年至2015年期间明尼苏达大学医院377例接受allo HSCT的患者,研究旨在阐明HLA匹配的同胞供者移植中CD34+细胞数量对HSCT预后的影响,根据CD34+数量将患者分为3组:T1,<5×106/kg;T2,5~7.5×106/kg;T3,≥7.5×106/kg。研究发现,更多CD34+数量与造血干细胞更好的植入相关:所有患者中性粒细胞ANC植入的中位时间为 12 天(0-29天),多因素分析显示,CD34+细胞数量与ANC植入独立相关,T3 和 T2 组 ANC 植入率显著高于 T1组;所有患者血小板植入的中位时间为 19天(1-117天),多因素分析显示,CD34+细胞数量与血小板植入独立相关,T3 组血小板植入率最高。
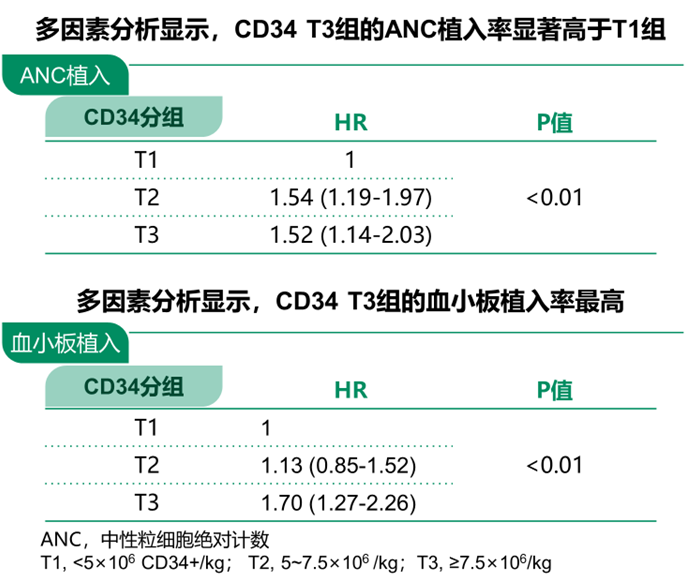
1.2 CD34+细胞数量与a/cGVHD风险息息相关
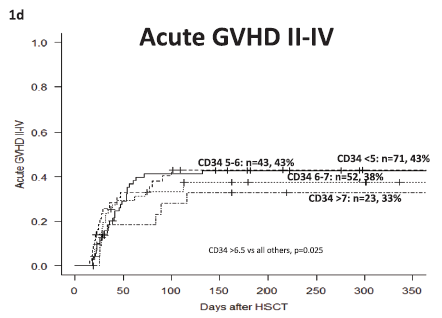
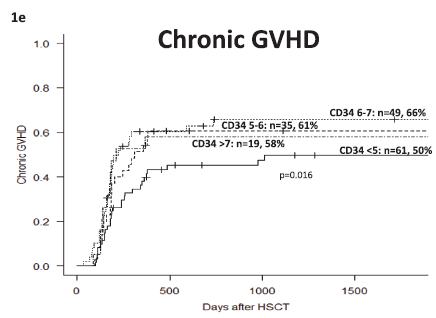
一项来自挪威奥斯陆大学医院的回顾性研究,分析了 189 名接受来自同胞供体的allo HSCT的恶性血液肿瘤患者,根据 CD34+细胞数量将患者分为四组:(2)<5×106 CD34+/kg(n=71)、(2)5-6×106 CD34+/kg(n=43)、(3)6-7×106 CD34+/kg(n=52)和(4)>7×106 CD34 +/kg(n=23)。所有患者II-IV 级aGVHD的累积发生率为 40%,其中接受6-7×106 CD34+/kg的患者II-IV级aGVHD的发生率(33%)最低,多因素分析显示,接受>6.5×106 CD34+/kg 的患者与较低的 II-IV级aGvHD 发生率相关(HR:0.50,95% CI:0.27-0.92,p=0.025)。所有患者II-IV 级cGVHD的累积发生率为 58%,其中接受 <5×106 CD34+/kg的患者cGVHD的发生率(50%)最低,多因素分析显示,接受<5×106 CD34+/kg 的患者与较低的 cGvHD 发生率相关(HR:0.57,95% CI:0.36-0.90,p=0.016)。
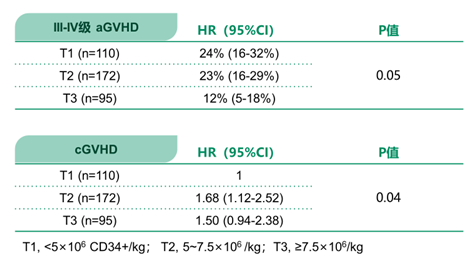
同样,在1.1中明尼苏达大学医院这项研究中,单因素分析显示(未进行多因素分析,不符合其标准),接受最高 CD34+细胞数量≥7.5×106/kg的患者,III-IV 级aGVHD的发生率显著较低。多变量分析显示,较多的 CD34 细胞数量与cGVHD风险增加存在显著相关。
1.3 CD34+细胞数量与OS息息相关
在1.1中明尼苏达大学医院的这项研究中,根据CD34+数量将377名接受HLA匹配的同胞供者allo HSCT的患者分为3组:T1<5×106/kg、T2 5-7.5×106/kg、T3≥7.5×106/kg,对不同CD34+细胞数量对HSCT预后的影响进行分析。多变量分析发现,较多的CD34+细胞数量与移植后更优的5年OS 相关:与 T1 组相比,T3 和 T2 组与更优的 5 年 OS 相关(T3:HR,0.57 [95% CI,0.38- 0.84];T2:HR,0.66 [95% CI,0.48-0.92];P=0.01)。
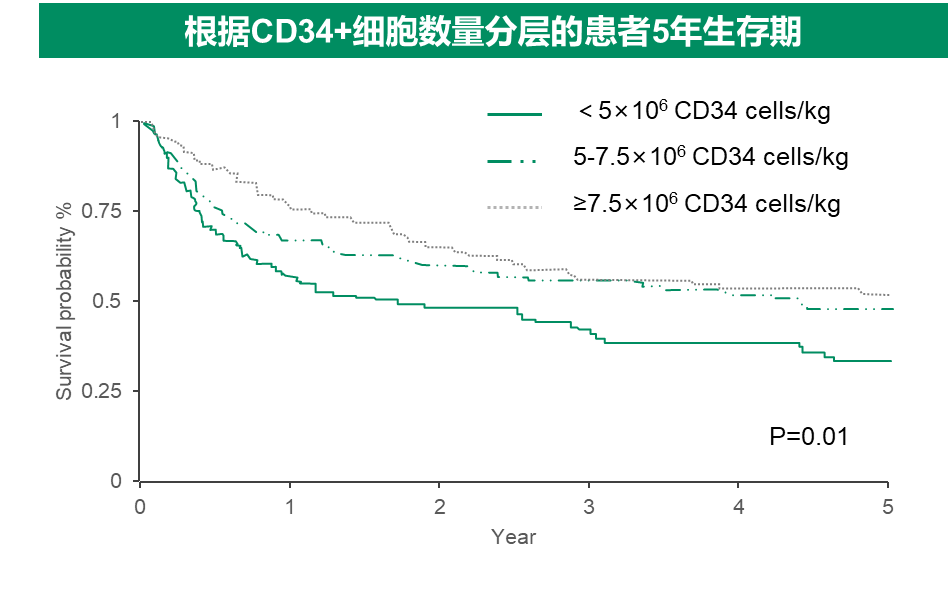
在1.2中挪威奥斯陆大学医院的回顾性研究纳入了 189 名接受来自同胞供体的allo HSCT的恶性血液肿瘤患者,多变量分析显示,6-7×106/kg 的 CD34 细胞数量与更优的 OS(HR:0.43,95% CI:0.25–0.77,p=0.004 )和更低的移植相关死亡率 TRM(HR:0.41,95% CI:0.18–0.92,p=0.03)相关。
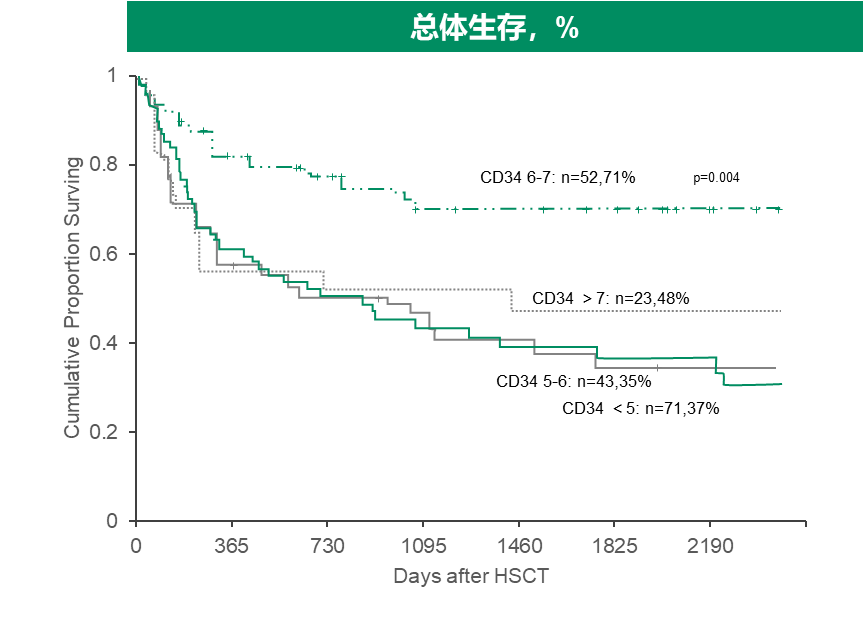
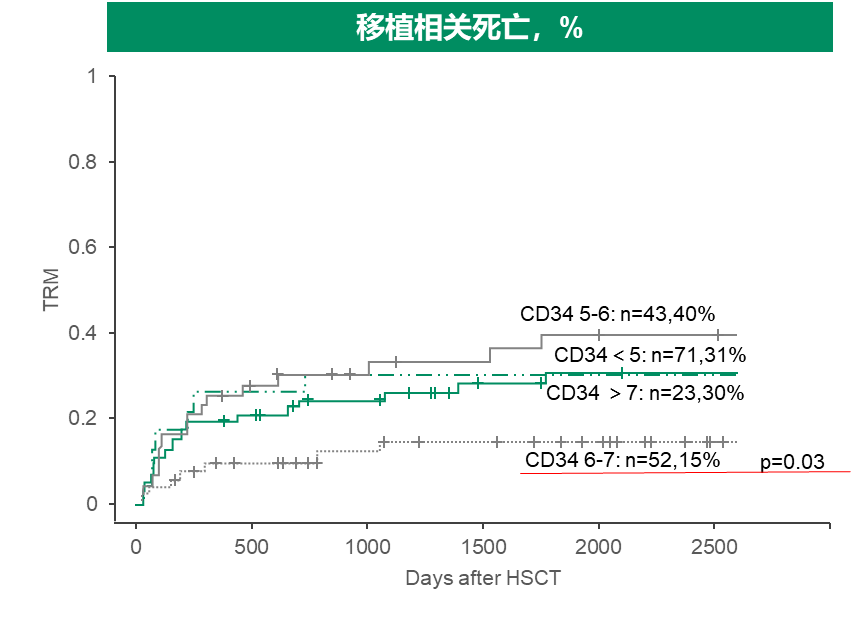
1.4 移植物中免疫细胞亚群组成与a/cGVHD同样息息相关
GVHD仍然是allo HSCT 的一大挑战,确切的发病机制目前尚未完全了解,涉及细胞因子和免疫细胞的复杂相互作用,临床实践中,我们更多地关注 CD34+和CD3+细胞数量,通常不会关注移植物中的免疫细胞组成。但是,不同患者HSCT移植物的免疫细胞群组成存在很大差异,这种差异与HSCT的预后有关,而这种差异取决于供者及干细胞采集方法,对移植物免疫细胞组成的详细分析可用于HSCT的风险评估,并为GVHD的防治提供新思路。
一项来自芬兰图尔库中心医院的回顾性研究,共纳入50例接受allo HSCT的AML患者,46/50(94%)名患者接受了10-12/12 HLA 匹配供者的HSCT,对患者接受移植物中主要免疫细胞群组成与临床结局之间的关系进行分析。该研究结果显示,发生II-IV级aGVHD 的AML患者接受的移植物中 CD3+T淋巴细胞的比例更高(p=0.007)且CD3+比例高低与 aGVHD 的严重程度正相关(p=0.028,Kruskal-Wallis 检验)。与 I级或无 aGVHD 的患者相比,患有 I-IV级aGVHD的患者接受的移植物中CD4+(p =0.039)、CD8+ p=0.032)、CD19+(p=0.044)和CD123+(p=0.011)细胞占比更高,其中,CD8+和CD123+在预测因子中排名靠前,证明它们在aGVHD发生中起到非常明显的作用。
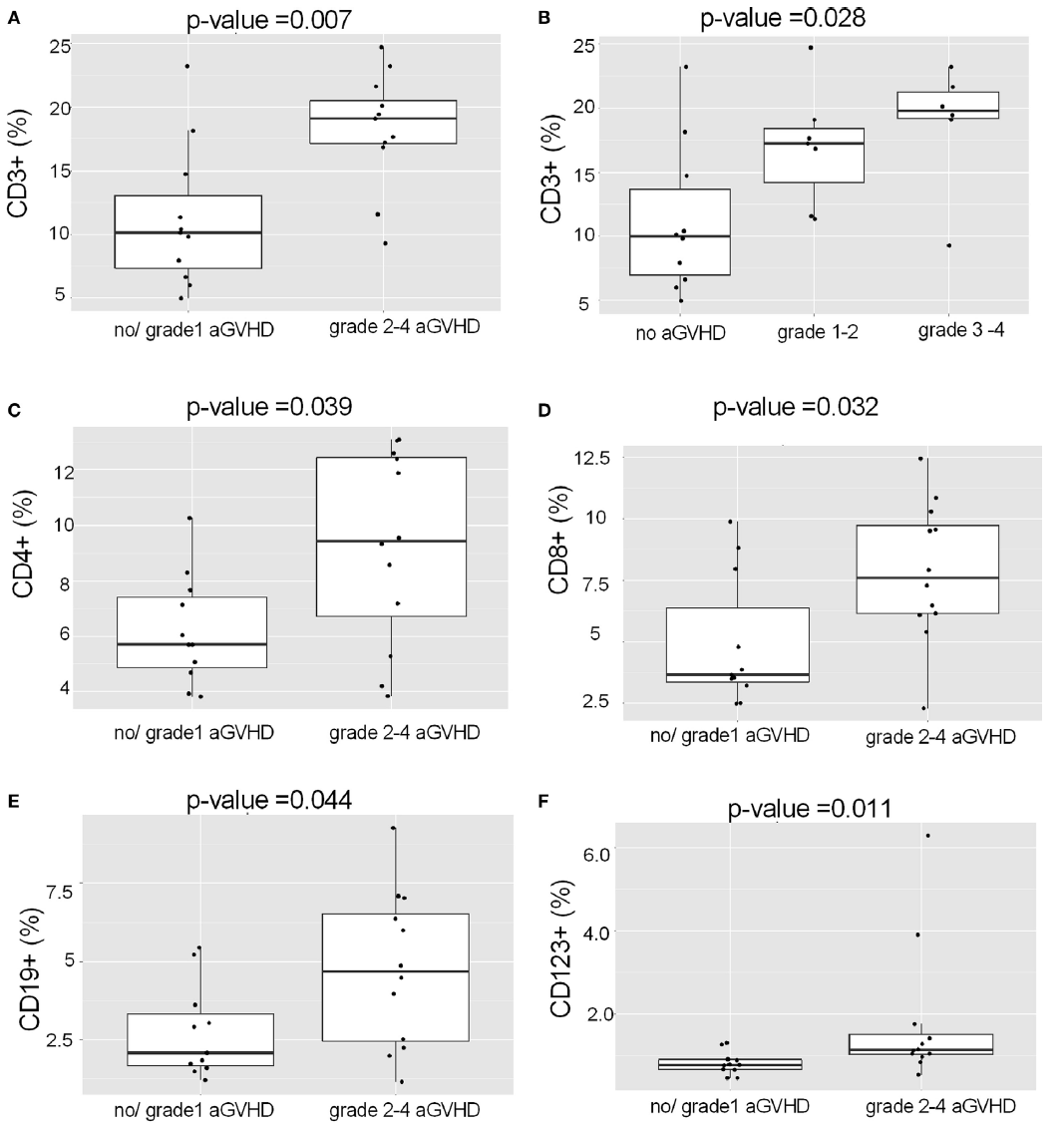
同时研究还发现,患有cGVHD 的AML 患者接受的 HSCT 移植物中的单核细胞比例明显低于未患 cGvHD 的患者(p=0.005),单核细胞被认为是 cGVHD 最重要的预测因子。
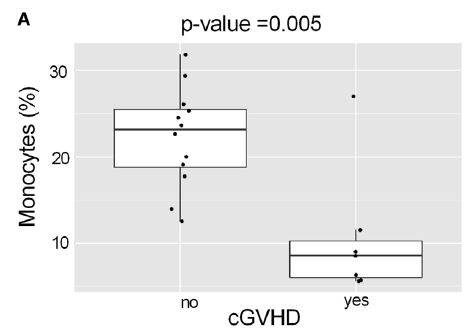
1.5 ABO血型不相容可导致HSCT多种并发症
ABO 不相容在 HSCT 中很常见,大约30-50%,其中10-15%的病例会出现临床显著的溶血。ABO血型不匹配可能会导致HSCT发生严重的临床并发症,包括急性溶血反应、植入延迟和纯红细胞再生障碍性贫血(PRCA)。
1.6 移植物中的中性粒细胞与allo HSCT并发症同样有关联
中性粒细胞的多种效应功能(胞外诱捕网NET、ROS的产生、抗原提呈、跨内皮迁移)参与了allo HSCT并发症如移植相关血栓性微血管病、aGVHD、cGVHD及CMV再激活等的发生发展。
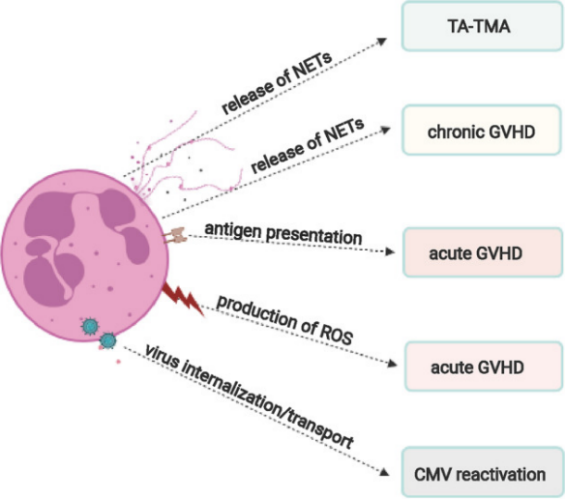
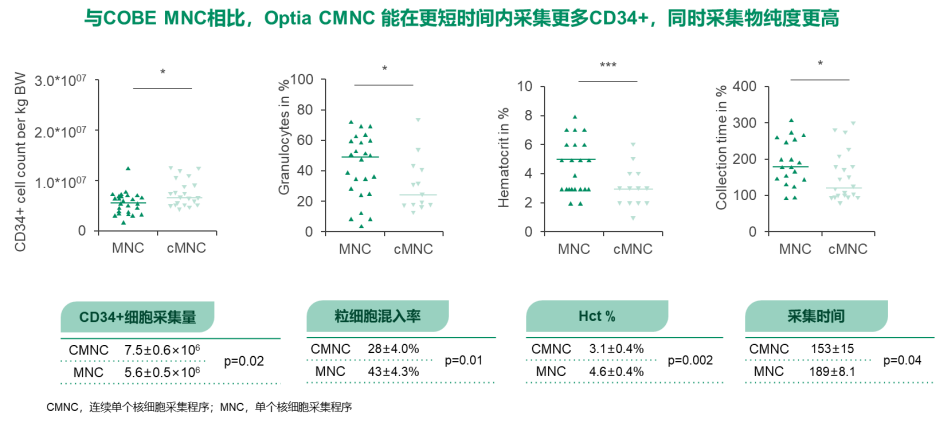
1.7 Spectra Optia CMNC程序在外周血造血干细胞采集中优势明显
Spectra Optia连续单个核细胞采集程序(CMNC)通过智能的界面自动管理(AIM)系统实时监测、反馈和调节采集界面,极大提升了CD34+细胞的采集效率,同时兼顾有效降低采集物RBC和粒细胞的混入率。在一项血液分离设备供者外周血造血干细胞的采集效果临床研究中,与COBE spectra MNC程序相比,Spectra Optia CMNC程序采集的CD34+数量更多,并且所用采集时间更短,同时采集物纯度更高(Hct及粒细胞混入率更低)。
2. T淋巴细胞采集对CAR-T
2.1 T淋巴细胞数量对CAR-T制备的影响
目前公开的 CAR-T 细胞临床试验描述中缺乏明确的单采标准,不同CAR-T细胞产品制备要求有所不同:目标细胞>1-4×109 T淋巴细胞或5-10×109单个核细胞。未采集到足够的T淋巴细胞是CAR-T治疗不能持久缓解的第一个障碍,目前许多患者由于先前化疗导致的淋巴细胞减少症被排除在 CAR T 细胞疗法之外。虽然CAR-T细胞制备工艺的改进提升可能会降低采集细胞数量的要求,但从临床医生的角度来看,至关重要的是要有明确的目标来优化起始细胞产品,最大限度地降低制造失败的风险。随着细胞治疗进一步的发展,期望有更多的临床指南出台规范指导淋巴细胞单采,进而规范细胞治疗的全流程质量管控。
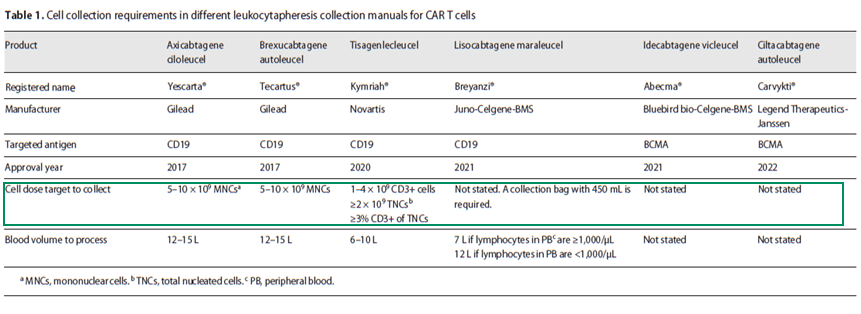
2.2 RBC污染可降低淋巴细胞活性
线粒体的完整性和功能对于细胞存活、干细胞能力和祖细胞迁移至关重要,线粒体膜电位降低提示细胞活性下降。一项心血管再生疗法试验中,研究用于急性心肌梗死后的心肌重塑与功能恢复的骨髓来源祖细胞的活性和功能之间的关系,该研究发现混入的RBC越多淋巴细胞的线粒体膜活性明显越低,提示RBC污染程度与淋巴细胞活性呈剂量依赖性降低的关系。而在国内CAR-T制备环节中,淋巴细胞从医院单采完成后,运输至上海或苏州等异地的工厂开始后续操作往往超过24小时,超过24小时后RBC对淋巴活性的负面影响更大。
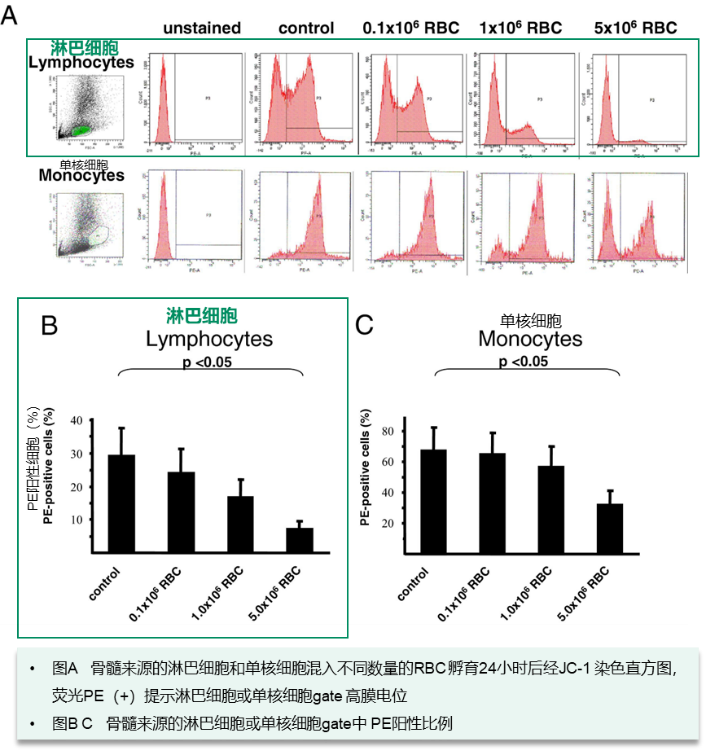
2.3 RBC污染不利于T淋巴细胞扩增及表型分化
目前,大多数CAR-T细胞和其他过继性T细胞疗法(ACT)都需在补充有 AB 型或O型供体人血浆的培养基中进行体外扩增。试验探究有无A1型红细胞(约90%A型血为A1型)的情况下,使用补充有O型血浆或 AB 型血浆的培养基扩增T淋巴细胞,同时增加含3%RBC的对照组,通过细胞计数、活力、流式细胞术表型等来分析T淋巴扩增、纯度、活力或表型分化有无差异。研究数据表明,不含RBC的培养物的倍数扩增明显高于含RBC的培养物(分别为90.1±33.4 和 67.3±24.8,p<0.005),含RBC的培养物中枢记忆T细胞TEM比例更高(分别为 84.43±6.50% 和 74.63±7.15%,p<0.005)。该研究发现:红细胞污染会不仅会降低淋巴细胞的扩增倍数,而且会影响T淋巴细胞表型分化的平衡,与血浆培养基中的同种凝集素滴度无关。

2.4 粒细胞污染可影响CAR-T细胞的转染及扩增
白细胞分离术收集的外周血单个核细胞(PBMNC) 作为自体CAR-T 制备的细胞来源,通常使用密度梯度分离、淘析或 T 细胞特异性抗体(磁珠法)来进行淋巴细胞富集。一项研究对两种 CAR-T 细胞(BCMA和 CD19)的制备过程中采用单变量分析密度梯度分离后PBMNC的组成对培养7天后CAR-T细胞扩增和特性的影响,该研究发现:CD3+ CAR T转染率与起始细胞材料的中性粒细胞和单核细胞数量呈负相关,CD3+细胞的扩增倍数与单核细胞的数量呈负相关。
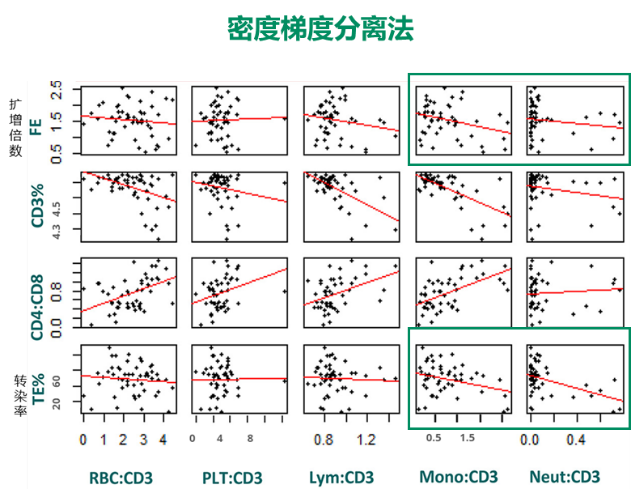
另一项研究对CD19-CAR T 细胞产品制备过程中使用抗 CD3/CD28磁珠富集法后分析PBMNC的组成与最终产品中T细胞和转染T细胞数量之间的关系,研究发现:CD19-CAR T患者的PBMC 浓缩物中粒细胞比例与 T细胞扩增(r=-0.362,P=0.097)和T细胞转染(r=-0.440;P=0.040)存在显著的负相关。
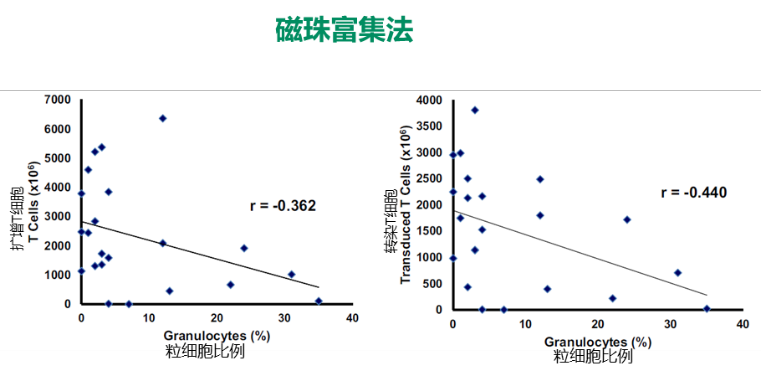
2.5 接受CAR-T治疗的患者血小板计数偏低会增加CRS的风险及血液毒性的严重程度
一项I/II 期临床试验纳入133 名接受CD19 CAR-T细胞治疗的复发/难治性B细胞恶性肿瘤患者(B-ALL,n=47;CLL,n=24;NHL,n=62),分析和确定患者CRS的发病率和严重程度相关的风险因素及生物标志物,从而可识别出适合早期干预的严重CRS风险高的患者。根据 CRS 严重程度对基线和治疗相关特征进行单变量和多变量分析发现,骨髓肿瘤负担高、淋巴细胞耗竭前血小板减少、使用环磷酰胺和氟达拉滨进行淋巴细胞耗竭、CAR-T 细胞剂量较高以及制造 CAR-T细胞时未进行中枢记忆CD8+分选是CRS的独立预测因素。

另一项多中心回顾性研究纳入并评估258 名接受 axicabtagene ciloleucel(axi-cel)或 tisagenlecleucel(tisa-cel)治疗复发/难治性大B细胞淋巴瘤患者的造血重建模式及潜在预测标志物,使用严重中性粒细胞减少症(ANC<500/µL)持续时间至+60 天作为主要终点来确定血液毒性的预测生物标志物。在训练队列(n=58)中,研究发现基线血细胞数量减少与中性粒细胞减少症持续时间的增加显著相关,其中与基线血小板计数减少的相关性尤其明显( r =−0.43; P =.001)。
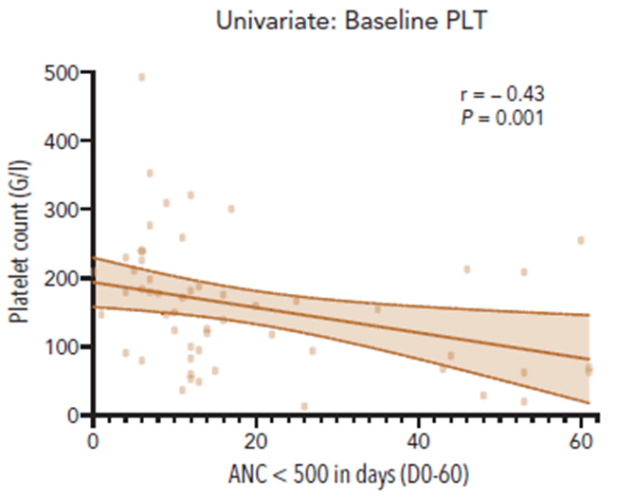
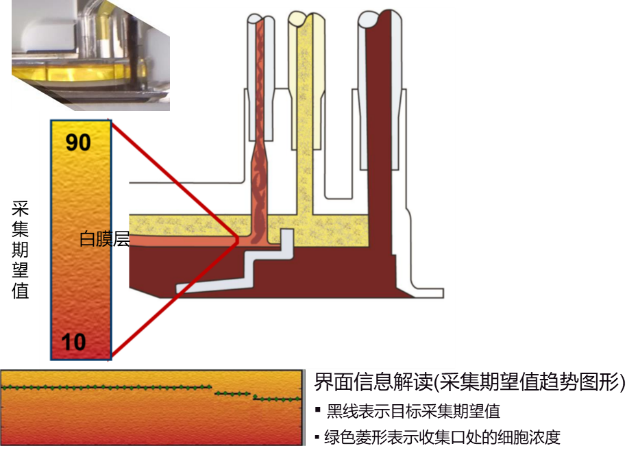
随着细胞免疫疗法的蓬勃发展,对外周血淋巴细胞的采集需求逐渐增加,淋巴细胞数量的充足性及RBC、粒细胞等污染程度,都会对CAR-T细胞的转染和扩增产生明确的影响,并且采集过程中血小板丢失可能会增加患者的治疗风险。以新一代Spectra Optia为代表的血液成分分离设备,其优秀的外周血淋巴细胞采集能力能为CAR-T细胞制备提供高质量的细胞基础,有效提升临床治疗效果及安全性。Spectra Optia装载了自动界面管理AIM系统,AIM使用独特的光学设备监测分离血液成分的界面位置和厚度,通过持续拍摄细胞收集口处的图像对细胞浓度的变化情况实时监测,并通过调整收集泵量化管理的界面位置(采集期望值:10-90)来优化白膜层内收集细胞时的深度。所以,相较于老一代设备COBE Spectra受限于操作者的主观经验,Spectra Optia不需要依靠操作者通过依靠肉眼对比采集管的颜色和所预期的WBC色卡Hct 含量颜色进行界面调整。
3. 治疗性单采在其他血液疾病治疗中也展现了广泛的应用前景
3.1 白细胞去除能安全有效地预防或减少WBC淤滞引起的急性并发症
一项多中心研究涵盖欧盟3家医院回顾性研究及中国8家医院前瞻性研究的综合数据,评估了Spectra Optia血液分离系统上对白细胞增多症患者进行白细胞去除程序(WBCD)的效果和安全性。研究一共进行了87次白细胞去除治疗,白细胞计数在WBCD术后总体下降了 50.3%,前瞻性研究中WBC下降比例(41.9%)低于回顾性研究(54.5%),主要原因可能是前瞻性研究中纳入的CML患者人数较多(12名/总计32名)。按疾病诊断分析,所有CML患者WBC下降比例只有27.7%,可能原因是CML患者的白血病细胞以成熟白细胞为主,密度更大,不易与血小板、红细胞完全分离。最常见的AE包括血小板减少症、低白蛋白血症、低钾血症、贫血、低钙血症和凝血酶原时间(PTT)延长。报告了 2 起严重不良事件(SAE),回顾性研究中的呼吸衰竭(n=1)和前瞻性研究中的脑出血(n=1),均与 Spectra Optia 设备无关。


3.2 PLT去除能安全有效地预防或减少PLT增多症相关急性并发症
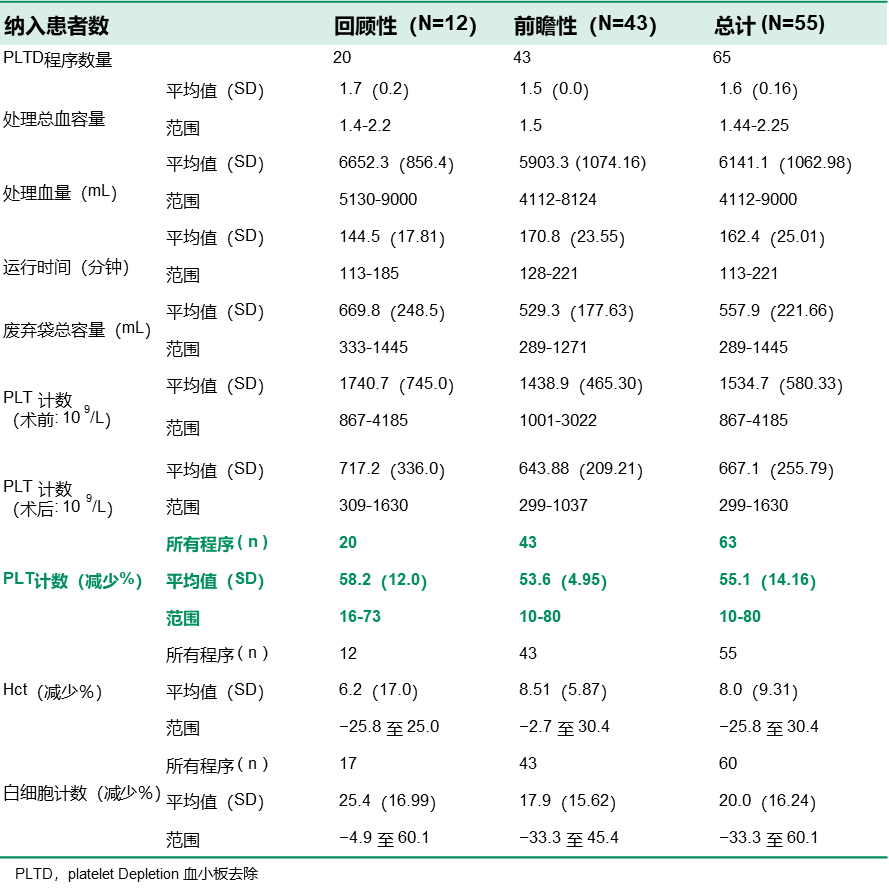
一线多中心回顾性+前瞻性研究评估了Spectra Optia血液分离系统上对PLT增多症患者进行 血小板去除程序PLTD的效果和安全性,其中涵盖欧盟2家医院回顾性研究及中国8家医院前瞻性研究的综合数据。所有患者的术前 PLT计数均较高(1534.7±580.3×109/L),PLT计数在PLTD术后平均下降55.1 ± 14.2%,最大下降幅度为 80%。研究中均未报告与 Spectra Optia 设备相关的 AE、SAE,均观察到了白细胞和红细胞丢失,平均白细胞和Hct减少百分比分别为 20.0±16.2% 和8.0±9.3%,主要原因是这些血液成分存在于PLT采集界面,预计患者在术中会损失非临床显著数量的白细胞和红细胞。如果在PLT去除术后观察到PLT几乎没有减少或没有减少,还可通过检测废液袋中的PLT计数来评估去除效果,可能的原因是在急性白血病患者的PLTD过程中,脾脏会补充血液循环血小板池以响应PLT的快速清除。
3.3 RBC去除能有效治疗原发性或继发性红细胞增多症
高原红细胞增多症(HAPC)是一种常见的继发性性红细胞增多症,青藏高原HAPC的发病率为5%~18%,红细胞增多会导致血液粘度显著增加和微循环障碍,从而导致组织缺氧、中风、睡眠障碍和心肌梗死等。
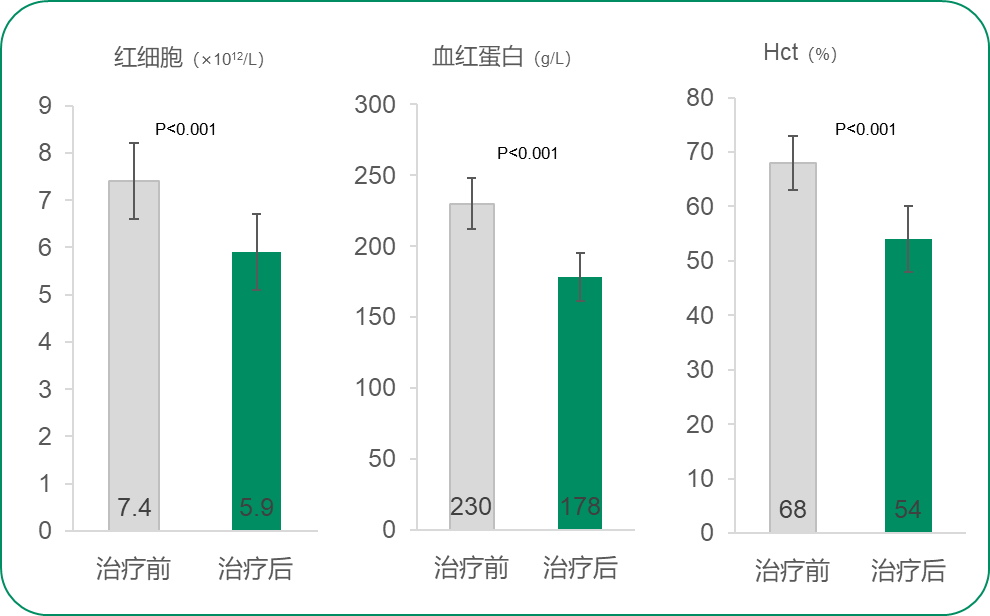
一项回顾性研究分析了西藏地区155例接受红细胞去除治疗的HAPC患者,通过比较治疗前后的常规血液检测值来评估治疗效果。患者接受去除治疗前后红细胞计数分别为7.4±0.8×1012/L和5.9±0.8×1012/L(P<0.001),血红蛋白浓度分别为230±18g/L和178±17g/L(P<0.001),Hct分别为 68±5% 和 54±6%(P<0.001),三者术后均出现明显降低。治疗前有凝血功能障碍的59例患者中,APTT由48秒缩短至36秒(P<0.001),PT由17秒缩短至12秒(P<0.001)。治疗前有高尿酸血症的78 例患者中,术后尿酸水平出现显著降低。(566 μmol/L vs 432 μmol/L,P<0.001)。
3.4 TPE联合多种疗法有效降低移植前患者DSA水平
对于移植前供者特异性抗体(DSA)阳性的患者,如果条件许可,建议更换供者。对于无合适供者可以替换时,可采取 DSA 脱敏治疗方案:如血浆置换、利妥昔单抗、依库珠单抗、硼替佐米、高剂量人血免疫球蛋白输注、供体血小板或“白膜层”(白细胞)输注等。TPE联合多种疗法降低移植前患者DSA水平可以参考以下血液移植中心DSA脱敏治疗方案。
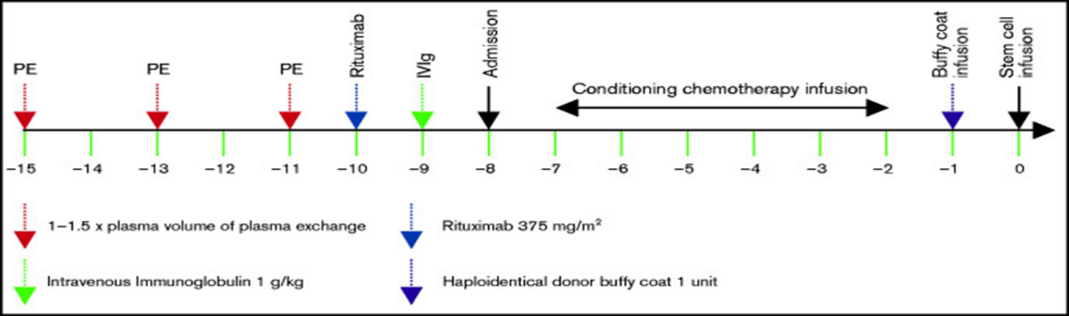
MD安德森癌症中心的DSA脱敏治疗方案参考:
-
连续三次隔日血浆置换(PE),每次血浆容量为1至1.5倍TBV,使用新鲜冰冻血浆或 4%-5% 人血浆白蛋白替换;
-
PE完成后的第二天,进行单剂量利妥昔单抗(Rituxan 375mg/m2 );
-
利妥昔单抗治疗后一天,进行1次IVIg治疗(1g/kg);
-
移植前一天,输注经辐照的白膜层,以中和剩余DSA。
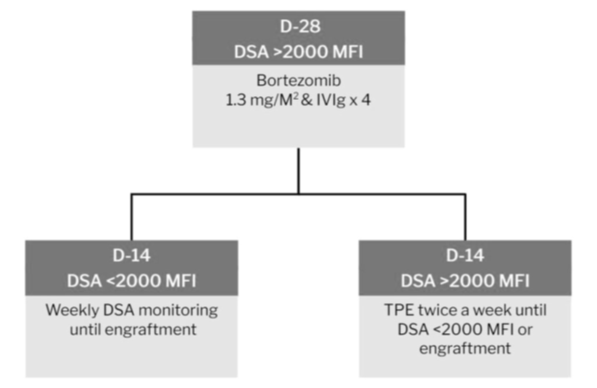
托马斯·杰斐逊大学金梅尔癌症中心的DSA脱敏治疗方案:(干细胞输注前四周实施)
-
每周监测DSA水平;
-
从D-28开始进行一疗程硼替佐米/IVIg治疗:硼替佐米 1.3mg/m2 和 IVIg 0.5g/kg,每周治疗2次,持续两周(第1、 4、8和11天);
-
从D-14开始,每周进行2次TPE,直到DSA水平下降至<2000 MFI
-
如果DSA水平已经<2000 MFI,继续监测DSA,直至造血干细胞植活
-
如果监测发现DSA水平回升>2000 MFI,则启动PE
-
如果DSA水平仍然>2000 MFI,将继续在预处理过程中继续每周进行2次PE,直到干细胞输注后DSA水平降至<2000 MFI或造血干细胞植活。
Spectra Optia作为新一代血液成分分离设备,凭借其高效、安全和精准的分离技术,在血液疾病治疗中展现了巨大的潜力。展望未来,随着技术的不断更新和临床应用的深入,Spectra Optia将为更多血液疾病患者带来福音,推动血液疾病治疗进入新的时代。






